薄层色谱法
薄层板的制作
市面上根据薄层层析板(如硅胶G板或聚酰胺板)的固定相标准颗粒大小分为不同规格,通常颗粒越细分离效果越好。制作时首先将吸附相(如硅胶)与少量惰性粘合剂(如硫酸钙)和水混合形成的浆状物,均匀地铺于以玻璃片、厚铝箔或塑料制成的载板上。铺过固定相的板先晾干,然后在烤炉内于110℃加热三十分钟进行活化。用于分析鉴定时吸附剂厚度一般为0.1–0.25毫米,而用于制备时(见下文)则为0.5–2.0毫米。
薄层层析技术
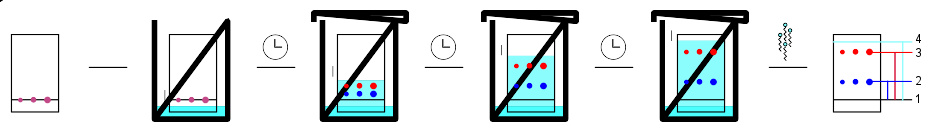
展开一个TLC板,一个紫色的斑点被分离为一个红色斑点与一个蓝色斑点
薄层层析的操作过程类似于纸色谱法,原理方面类似于柱色谱,因而与纸色谱相比具有很多优势,如它分离效果好,灵敏快速,对于固定相的选择更多,且TLC的结果还可作为柱层析的参考。由于以上的诸多优势,使薄层层析技术成为当今检测化学反应、定性分析化合物和分离化合物的最常用的手段。实验室常用的是硅胶薄层层析,其制作简单、成本低廉且用途广泛。在化学技术当中,符合这几点的技术方法并不多见。
分离的过程与原理
在混合物中,不同化合物会以不同的速率前进,其原因为吸引力及固定相的差异和样本溶质在溶剂里溶解度的差异。样本的分离(以Rf值来比较)结果是可以借由改变洗脱溶剂或使用的混合的洗脱溶剂来改变的。化合物的分离是利用化合物与流动相之间在固定相上竞争结合位所造成的。例如:使用硅胶做为固定相的话,此固定相可以被视为极性。此时加入两不同极性的化合物,极性较强的化合物与硅胶间会有较强作用力,因此,更能抵抗流动相并与硅胶结合;极性较弱的化合物与硅胶的作用能力较差,因此更容易流动,拥有更高的Rf值。如果流动相的极性变得更强的话,这样更能够抵抗化合物与胶上结合的能力,使所有TLC片上的化合物上升到更高的位置。这样的溶剂我们称为“强”溶剂(洗脱剂),而“弱”洗脱剂则几乎不能移动它们。“强”与“弱”的比较是取决于TLC片上的涂层(固定相)。以硅胶TLC片来说,洗脱剂的强度比较为:
全氟烷(最弱)<己烷<戊烷<四氟化碳<苯/甲苯<二氯甲烷<乙醚<乙酸乙酯<乙腈<丙酮<丙醇/正丁醇<水<甲醇<三乙胺<乙酸<甲酸(最强)
C18的相位与TLC相反。在应用上,使用乙酸乙酯和己烷的混合物做为流动相的话,加入更多的乙酸乙酯会使TLC片上所有化合物的Rf値升高。改变流动相的极性通常并不会使TLC片上的化合物的前后顺序发生改变。如果要使化合物的前后顺序发生改变的话,此时就应使用非极性的固定相来代替极性固定相,如C18-官能基硅胶。
操作
薄层色谱的步骤如下:
点样:将试样溶液用毛细管在层析板上距离板底部约1.5厘米的位置点若干下(次数根据样品浓度而定),并静置顷刻(或加热)以使溶剂完全蒸发。若溶剂难以挥发,则点样之后需要将板放于真空容器中干燥后再使用。溶剂的蒸发是必须的,否则残留的溶剂会与流动相作用,降低流动相的均一性,导致分离效果变差。
将少量合适的溶剂(流动相)倒于一个合适的玻璃器皿(展缸)中,让流动相高度不超过1厘米,并在上面放上表面皿使溶剂蒸气在展缸中饱和。可在展缸底部放上一张滤纸,让滤纸底部浸没于溶剂中并靠在展缸内壁,过几分钟后让洗脱溶剂蒸发并在展缸空间内饱和。若不经过以上步骤可能会导致分离度的下降或使结果不具重复性。
然后将层析板置于展缸内(样品点不可触碰溶剂表面),盖上盖子让溶剂通过毛细现象缓慢爬升。溶剂遇到样品混合点时,会带着样品上升(即洗脱样品)。当溶剂快到层析板顶端时,将板拿出,迅速记录溶剂到达的高度并晾干。不要让溶剂爬升到达板的顶部。
Rf值 (retention factor)
对于确定的固定相,混合物样品中不同的化合物在层析板上爬升的速度不同,这是由于它们对于固定相的吸附能力不同,对于洗脱剂的溶解能力也不同。改变不同的洗脱溶剂,或用不同溶剂配成混合洗脱剂,化合物的分离效果可自行调节。组分在板上的分离情况一般用比移值(Rf)的大小来表征。薄层色谱板上的分离情况还可用于预测柱层析或快速柱层析的分离效果。
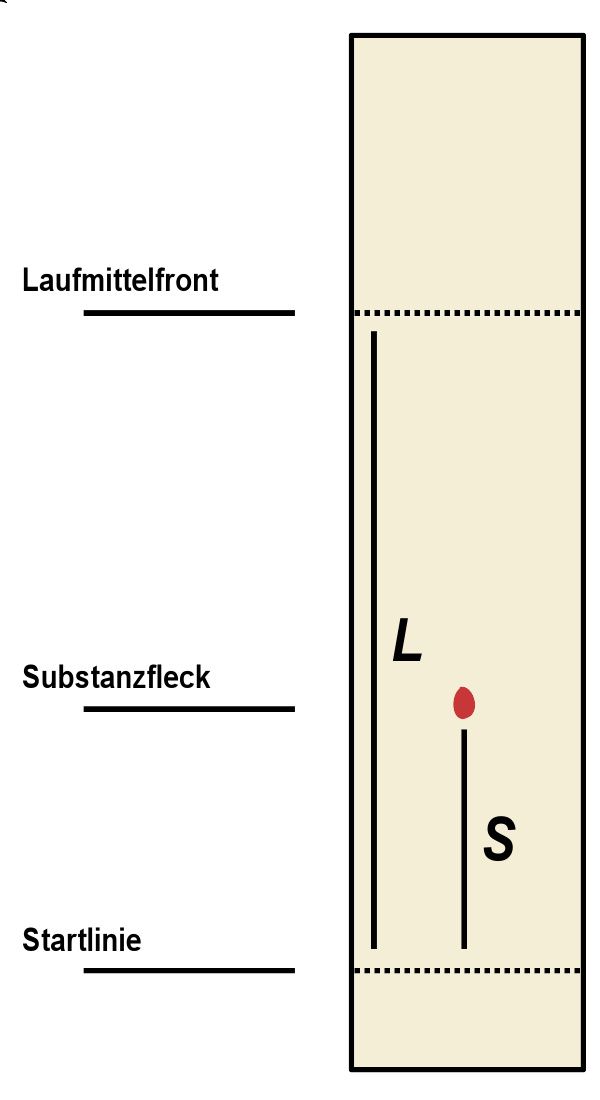
Rf值定义:Rf=S/L,其中L表示溶剂从原点至终点距离;S表示从原点至化合物前沿距离。图注: Startlinie = 样品的起始线 Substanzfleck = 样品中某成分的显色点 Laufmittelfront = 溶剂到达的位置
由于薄层色谱中很难产生均匀的吸附剂涂层,且薄板的质量与吸潮程度亦参差不齐,所以即便是同一物质在同类型而不同的层析板上得到的比移值也难以完全一致。相比于纸色谱这是薄层色谱的缺点。操作中常常将标准试样与试样在同一薄板上同时展开并点上混合点,以克服这一缺点。
化合物的分离是利用化合物与流动相之间在固定相上竞争结合位所造成的。例如:使用硅胶做为固定相的话,此固定相可以被视为极性。此时加入两不同极性的化合物,极性较强的化合物与硅胶间会有较强作用力,因此,更能抵抗流动相并与硅胶结合;极性较弱的化合物与硅胶的作用能力较差,因此更容易流动,拥有更高的Rf値。如果流动相的极性变得更强的话,这样更能够抵抗化合物与胶上结合的能力,使所有TLC片上的化合物上升到更高的位置。这样的溶剂我们称为"强"溶剂(洗脱剂),而"弱"洗脱剂则几乎不能移动它们。"强"与"弱"的比较是取决于TLC片上的涂层(固定相)。
洗脱剂(流动相)
以硅胶TLC片来说,洗脱剂的强度比较为:
而对于C18覆盖的TLC板,其顺序完全相反。在应用中,若使用乙酸乙酯/庚烷的混合溶剂作为流动相,乙酸乙酯比例越高会导致所有化合物在TLC上的Rf值更大。通常,更改流动相的极性不会导致TLC板上的化合物斑点前后顺序发生改变。若需要更改化合物在TLC板上的前后顺序,可以选用反相TLC板,即使用非极性固定相来代替极性固定相,如C18修饰后的硅胶。
制备TLC
TLC还可用于少量如100毫克左右的化合物的分离,此时混合物样品不是“点”在板上,而是涂抹在TLC板上且高于洗脱剂液面上的位置,形成一条水平的样品带。然后如同展开小型TLC板一样将制备TLC板展开并晾干,然后将每条携带不同化合物的色带从板上分别刮下,并用合适的溶剂萃取洗涤(如二氯甲烷)并过滤掉固定相等不溶物,得到滤液后再脱除溶剂就得到纯净的化合物。对于小量且易于分离的反应产物,制备TLC较柱层析在时间、效率和经济上更占优势。显然,这种方法得到的TLC板不可用全部用化学方法显色,否则会导致样品全部损失。因此可使用一些不会破坏样品的显色方法,如紫外线。或者,可刮下板上部分的吸附相进行鉴定,也可以割分的TLC板用显色剂(如碘)找到需要的化合物。
分析与显色
由于被分离出的化学品可能是无色的,因此下列几种方法可用于让没有可见光吸收的斑点显色:
通常在可使用少量的荧光化合物,如锰-活化的锌硅酸盐加入到吸附相当中,使得吸附物在黑光(UV254)下可以显色。固定相在荧光下本身显绿色,因此化合物的斑点可以掩盖掉荧光下的绿色从而达到显色目的。
碘蒸气是对于大多数化合物都是显色试剂
许多化合物的斑点可以通过将TLC板浸没于下列显色剂当中而达到显色目的,如:高锰酸钾,碘,溴,磷钼酸,茴香醛法与茚三酮。
脂类的情况下,色谱图可能会被转移到PVDF膜上,然后受到进一步的分析,如质谱法,这种技术称为Far-Eastern blotting。
当显色成功后,就可以计算出Rf值,或保留因子。其计算方法是测量每个点从原点到达最终停留位置的距离除以原点到溶剂前沿的距离。这些值取决于使用的溶剂与TLC板的材质,而与物理常数无关。
应用与实例
在有机化学中,有机反应可通过TLC进行定性的检测。使用毛细管将样品点于TLC板上:一个点表示起始原料,一个点表示反应体系,一个点表示两者“混合点”。一个小型TLC板(3X7cm)只需几分钟就可以完全展开。整个分析过程是定性的,它可显示起始原料是否消失即是否反应已经完成;是否有产物出现以及产生了多少产物。需注意的是,从低温环境中取样的TLC结果可能会出现误差,因为样品的温度在毛细管中就已经升至室温,其与低温反应瓶内的反应将不一样。例如DIBAL-H还原酯制备醛的反应。
以下是一个实例:使用薄层层析法分离绿叶的提取物(如菠菜)的7个阶段。胡萝卜素洗脱的速度很快因此只能在第二步中看到。叶绿素A和B在最后一步的中间位置,叶黄素是保持黄色的第一个斑点。
参见
氟代脱氧葡萄糖
Template:层析法
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

相关资料

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读


知识互答
关于我们

APP下载



























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}