



结构生物学
研究方法
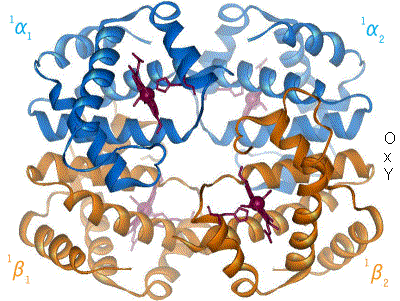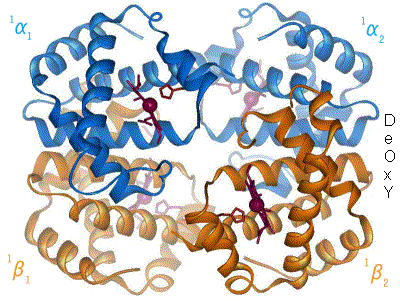
血红蛋白,红血球中发现的氧气运输蛋白质
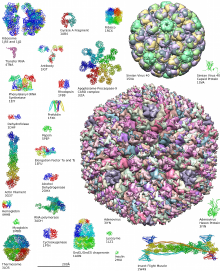
蛋白质数据库(PDB)中蛋白质结构的一些例子。
由于生物大分子的直径一般为数个纳米到数百个纳米,即使用最先进的光学显微镜也因为太小而无法进行观测。因此结构生物学家发展了各种方法来研究生物大分子的结构。目前用于研究生物大分子三维结构常用的实验手段包括:
质谱法
X射线晶体学
蛋白质核磁共振光谱法 ( 英语 : Nuclear magnetic resonance spectroscopy of proteins ) (NMR)
电子自旋共振(EPR)
蛋白酶解
低温电子显微镜 ( 英语 : Cryo-electron microscopy )
原子力显微镜
小角散射 ( 英语 : Small-angle scattering )
多角度光散射 ( 英语 : Multiangle light scattering )
超快激光光谱学 ( 英语 : Ultrafast laser spectroscopy )
双极化干涉仪 ( 英语 : Dual-polarization interferometry ) ,和圆二色性
所有的这些研究方法都有其优点和缺陷,不同的研究对象需要采用不同的方法。如核磁共振光谱学比较适合研究小分子量(通常小于20kDa)的蛋白和蛋白相互作用位点的信息,而电子显微学比较适合研究超大分子量蛋白复合物(通常远大于100kDa)甚至亚细胞器的结构;因此往往需要通过结合不同的方法来互补。
在过去的几年中高度精确的物理分子模型已经成为可能,以补充在生物结构的在硅片的研究。这些模型的实例可在蛋白质数据库(PDB)中找到。
相关的诺贝尔奖
佛朗西斯·克里克和詹姆斯·沃森在DNA分子的结构研究上的贡献而获得了1962年诺贝尔生理学和医学奖;
马克斯·佩鲁茨和约翰·肯德鲁因为利用X射线晶体学研究了肌红蛋白的三维结构而获得了1962年诺贝尔化学奖;
多萝西·克劳福特·霍奇金因为通过X射线晶体学确定了一些重要生化物质的结构而获得了1964年诺贝尔化学奖;
亚伦·克拉格因为在利用电子晶体学测定生物物质的结构方面的贡献而获得了1982年诺贝尔化学奖;
赫伯特·豪普特曼和杰罗姆·卡尔勒因为在测定晶体结构的直接方法上的贡献而获得了1985年诺贝尔化学奖;
约翰·戴森霍费尔、罗伯特·胡贝尔和哈特姆特·米歇尔因为在解析光合作用中心的三维结构上的贡献而获得了1988年诺贝尔化学奖;
保罗·博耶和约翰·沃克因为在研究ATP酶结构方面的贡献而获得了1997年诺贝尔化学奖;
库尔特·维特里希因为发明了利用多维核磁共振技术测定溶液中生物大分子三维结构的方法而获得了2002年诺贝尔化学奖;
罗德里克·麦金农由于在细胞膜离子通道的结构和机理研究方面的贡献而获得了2003年诺贝尔化学奖;
罗杰·科恩伯格因为在真核转录的分子基础研究上的贡献而获得了2006年诺贝尔化学奖;
文卡特拉曼·拉马克里希南、托马斯·施泰茨和阿达·约纳特由于对核糖体结构和功能方面的研究而获得了2009年诺贝尔化学奖;
罗伯特·莱夫科维茨和布莱恩·科比尔卡由于对G蛋白偶联受体的研究而获得了2012年诺贝尔化学奖;
参见
生物物理学
生物化学
结构基因组学
立体化学
X射线晶体学
核磁共振波谱法
电子显微学
三维结构
蛋白质结构预测
施一公
参考文献
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

相关资料

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
关于我们

APP下载




















