钽
历史
1802年,安德斯·古斯塔夫·埃克贝格(Anders Gustaf Ekeberg)在瑞典发现了钽元素。一年之前,查理斯·哈契特发现钶元素(Columbium,后改名为铌)。 1809年,英国化学家威廉·海德·沃拉斯顿(William Hyde Wollaston)对钽和钶的氧化物进行了对比,虽然得出不同的密度值,但他认为两者是完全相同的物质。 德国化学家弗里德里希·维勒其后证实了这一结果,因此人们以为钽和钶是同一种元素。另一德国化学家海因里希·罗泽(Heinrich Rose)在1846年驳斥这一结论,并称原先的钽铁矿样本中还存在着另外两种元素。他以希腊神话中坦塔洛斯的女儿尼俄伯(Niobe,泪水女神)和儿子珀罗普斯(Pelops)把这两种元素分别命名为“Niobium”和“Pelopium”。 后者其实是钽和铌的混合物,而前者则与先前哈契特所发现的钶相同。
1864年,克利斯蒂安·威廉·布隆斯特兰(Christian Wilhelm Blomstrand)、 亨利·爱丁·圣克莱尔·德维尔和路易·约瑟夫·特罗斯特(Louis Joseph Troost)明确证明了钽和铌是两种不同的化学元素,并确定了一些相关化合物的化学公式。 瑞士化学家让-夏尔·加利萨·德马里尼亚(Jean Charles Galissard de Marignac) 在1866年进一步证实除钽和铌以外别无其他元素。然而直到1871年还有科学家发表有关第三种元素“Ilmenium”的文章。 1864年,德马里尼亚在氢气环境中加热氯化钽,从而经还原反应首次制成钽金属。 早期炼成的钽金属都含有较多的杂质。维尔纳·冯·博尔顿(Werner von Bolton)在1903年首次制成纯钽金属。钽曾被用作电灯泡灯丝,直到被钨淘汰为止。
科学家最早使用分层结晶法把钽(七氟钽酸钾)从铌(一水合五氟氧铌酸钾)中提取出来。这一方法由德马里尼亚于1866年发现。今天科学家所用的则是对含氟化物的钽溶液进行溶剂萃取法。
性质
物理属性
钽是一种灰蓝色 高密度坚硬金属,具高延展性、导热性和导电性。钽能抵抗酸的腐蚀,它在150 °C以下甚至能够抵抗王水的侵蚀。能够溶解钽的物质包括:氢氟酸、含氟离子和三氧化硫的酸性溶液以及氢氧化钾溶液。钽的熔点高达3017 °C(沸点5458 °C),只有钨、铼、锇和碳的熔点比它更高。
钽有两种晶体相,分别称为α和β。其中α态柔软,具延展性,晶体结构为体心立方(空间群为 Im3m ,晶格常数 a = 0.33058 nm),努普硬度为200至400 HN,电阻率为15至60 µΩ⋅cm。β态则坚硬易碎,晶体结构属于四方晶系(空间群为 P42/mnm , a = 1.0194 nm, c = 0.5313 nm),努普硬度为1000至1300 HN,电阻率为170至210 µΩ⋅cm。β态是一种亚稳态,在加温至750至775 °C后会转变为α态。钽金属块几乎完全由α态晶体组成,β态通常以薄片形式存在,可经磁控溅射、化学气相沉积或从共晶液态盐电化学沉积而得。
化学属性
钽可以形成氧化态为+5和+4的氧化物,分别为五氧化二钽(Ta 2 O 5 )和二氧化钽(TaO 2 ), 其中五氧化二钽较为稳定。 五氧化二钽可以用来合成多种钽化合物,过程包括将其溶解在碱性氢氧化物溶液中,或与另一种金属氧化物一同熔化。如此形成的物质有钽酸锂(LiTaO 3 )和钽酸镧(LaTaO 4 )等。在钽酸锂中,钽酸离子 TaO − 3 并不出现,这其实代表 TaO 7− 6 所形成的八面体钙钛矿骨架结构。钽酸镧则含有单个 TaO 3− 4 四面体基。
氟化钽可以用来从铌当中分离出钽元素。 钽的卤化物可以有+5、+4和+3氧化态,分别对应 TaX 5 、 TaX 4 和 TaX 3 型的化合物,另外还存在多核配合物以及亚化学计量化合物。 五氟化钽(TaF 5 )是一种白色固体,熔点为97.0 °C;五氯化钽(TaCl 5 )也是白色固体,熔点为247.4 °C。五氯化钽可以被水解,且在高温下可与更多的钽反应,形成吸湿性很强、呈黑色的四氯化钽(TaCl 4 )。钽的五卤化物可以用氢还原成三卤化物,但无法进一步还原成二卤化物。 钽﹣碲合金会形成准晶体。 2008年一份文章表示存在氧化态为−1的钽化合物。
与其他难熔金属一样,最坚硬的钽化合物是其氮化物和碳化物。碳化钽(TaC)与碳化钨相似,都是十分坚硬的陶瓷材料,常被用于制造切割工具。氮化钽(III)在某些微电子生产过程中被用作薄膜绝缘体。 美国洛斯阿拉莫斯国家实验室的化学家研发出了一种碳化钽﹣石墨复合材料,这是人们已知最坚硬的物质之一。韩国科学家研发了一种比常见钢合金强2至3倍的无定形钽﹣钨﹣碳合金,其柔韧度也比钢更高。 铝化钽有两种:TaAl 3 和Ta 3 Al。两者均稳定、耐火、反射率高,因此有可能可用作红外线反射镜涂层。
同位素
自然产生的钽由两种同位素组成: Ta(0.012%)和 Ta(99.988%)。 Ta是一种稳定同位素。 Ta(“m”表示亚稳态)有三种理论预测的衰变方式: 内转换至基态 Ta,β衰变成 W,或经电子捕获形成 Hf。不过,尚未有实验证明该同核异构体具有放射性。其半衰期至少有10 年。 Ta基态的半衰期只有8小时。 Ta是唯一一种自然产生的钽同核异构体,也是全宇宙最稀有的同位素(经其他元素衰变产生及宇宙射线产生的短寿命同核异构体除外)。
钽可以作为盐弹的“盐”(铬是另一种“盐”)。盐弹是一种假想的大杀伤力核武器。其外层(所谓的盐)由 Ta组成,会因内部核弹爆炸所产生的高能中子流而嬗变成 Ta。这一同位素的半衰期为114.4天,衰变时产生112万电子伏特(即1.12 MeV)的伽马射线。这可大大加强爆炸后数月之内辐射落尘的危害性。这种盐弹从未投入生产或测试,也因而未曾在战争中使用过。
存量

澳洲皮尔布拉地区开采的钽铁矿
钽在地球地壳中的含量依重量计约为百万分之1 至2 。钽矿物有许多种,其中钽铁矿、细晶石、锡锰钽矿、黑稀金矿、复稀金矿等可作为工业钽开采的原石。钽铁矿(Fe,Mn)Ta 2 O 6 是最重要的钽原石。钽铁矿的结构和钶铁矿(Fe, Mn) (Ta,Nb) 2 O 6 相同。如果矿物中的钽比铌更多,则称钽铁矿,相反则称钶铁矿(或铌铁矿)。钽及其矿物的密度都很高,所以最适宜用重力分离方法进行萃取。其他含钽矿物还有铌钇矿和褐钇铌矿等等。
钽的开采主要集中在澳洲,环球卓越金属(Global Advanced Metals)在西澳大利亚拥有两座矿场,一座位于西南部格林布什,另一座位于皮尔布拉地区的沃吉纳。 巴西和加拿大是铌的主要产国,当地的矿石开采也会产出少量的钽元素。另外,中国、埃塞俄比亚和莫桑比克也是重要的钽产国。钽在泰国和马来西亚是锌开采过程的副产品。 未来估计最大的钽来源依次为:沙特阿拉伯、埃及、格林兰、中国、莫桑比克、加拿大、澳洲、美国、芬兰及巴西。
钶铁矿和钽铁矿合称钶钽铁矿, 在中非有一定的存量。第二次刚果战争就与此有关。根据2003年10月23日的一份联合国报告, 钶钽铁矿的走私和运输使得当地战争得以持续。该战争自1998年以来已导致约540万人死亡, 是第二次世界大战以来死伤最为严重的军事冲突。刚果盆地战地的钶钽铁矿开采所引发的企业道德、及环境生态问题成为广受关注的议题。 虽然钶钽铁矿开采对刚果经济十分重要,但是刚果的钽产量却只是世界总产量的很少一部分。根据美国地质调查局的年报告,该地区的钽产量在2002至2006年期间占了不到世界总量的1%,在2000及2008年也只达到10%。
根据目前的趋势预测,所有钽资源在50年以内会消耗殆尽,因此急需加大回收再用。
生产
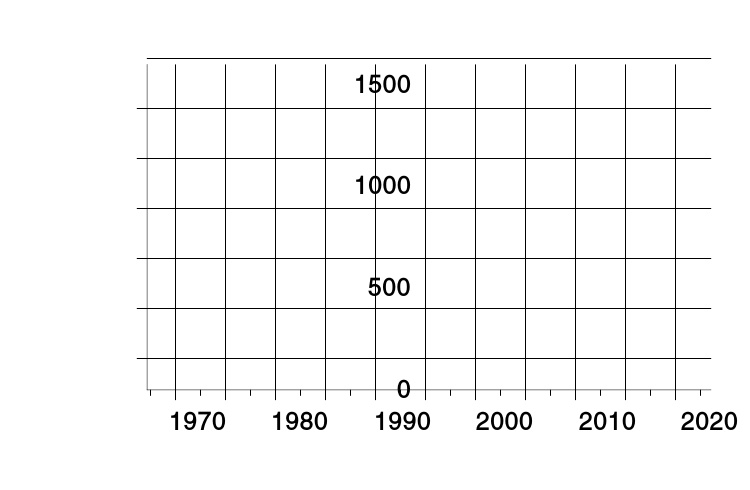
截止2012年的钽生产趋势
钽从钽铁矿中的萃取过程有多个步骤。首先原石在压碎后经重力分离提高钽矿物的含量。这一步一般在矿场附近进行。
化学提炼
钽矿石一般含有大量铌元素,因此两者都会经提炼后出售。整个湿法冶金过程由淋洗开始,矿石浸溶在氢氟酸和硫酸中,产生水溶氢氟化物。这样就可以把钽从各种非金属杂质中分离出来。
氢氟化钽和氢氟化铌可经溶剂提取法从水溶液中提取出来,适用的有机溶剂包括环己酮和甲基异丁基酮。这一步会移除各种金属杂质(如铁、锰、钛、锆)的水溶氟化物。通过调节pH值可将钽从铌中分离出来。铌在有机溶剂中需较高的酸度才可溶解,因此在酸度较低的环境下可以轻易地移除。剩余的纯氢氟化钽溶液在经氨水中和之后,会形成氢氧化钽(Ta(OH) 5 ),煅烧后产生五氧化二钽(Ta 2 O 5 )。
氢氟化钽还可以与氟化钾反应形成七氟钽酸钾(K 2 [TaF 7 ])
它与钠在800 °C左右的熔融盐中会发生还原反应,从而制成钽金属。
更早期的一种分离方法在氢氟化物混合溶液中加入氟化钾,这种过程叫做德马里尼亚过程。
这样产生的K 2 [TaF 7 ]和K 2 [NbOF 5 ]具有不同的水溶性,所以能利用分离结晶法分开。
电解
钽的电解提炼方法与霍尔-埃鲁电解炼铝法相似。与其不同的是,钽的电解提炼法的起始氧化物和金属产物都不是液态,而是固态粉末。这一方法由剑桥大学科学家于1997年发现。他们将少量金属氧化物置于熔融盐中,并用电流对其进行还原。阴极是金属氧化物的粉末,而阳极则由碳组成。电解质是处于1000 °C的熔融盐。首个利用这种方法的精炼厂可产出全球钽需求量的3至4%。
加工
钽的焊接必须在氩气或氦气等惰性环境下进行,以避免空气中其他气体对其造成污染。钽不可软焊,也很难磨碎,特别是已退火的钽金属。已退火的钽可延展性极高,能轻易制成薄片。
应用
电子

钽电解电容
钽的最大应用是用钽粉末制成的电子元件,以电容器和大功率电阻器为主。钽电解电容利用钽能够形成氧化物保护层的原理,以压制成圆球状的钽粉末作为其中一块“偏板”,以其氧化物作为介电质,并以电解质溶液或固体导电体作为另一块“偏板”。由于介电质层非常薄,所以每单位体积内能够达到很高的电容。这样的电容器体积小、重量轻,很适用于作为手提电话、电脑以及汽车内的电子元件。
合金
钽可用来制造各种熔点高的可延展合金。这些合金可作为超硬金属加工工具的材料,以及制造高温合金,用于喷射引擎、化学实验器材、核反应堆以及导弹当中。 钽具有高可延展性,能够拉伸成丝。这些钽丝被用于气化各种金属,如铝。钽可以抵御生物体液的侵蚀,又不会刺激组织,所以被广泛用来制造手术工具和植入体。例如,钽可以直接与硬组织成键,因此不少骨骼植入物都有多孔钽涂层。
除了氢氟酸和热硫酸之外,钽能抵抗几乎所有酸的腐蚀。因此钽可以作化学反应容器以及腐蚀性液体导管的材料。氢氯酸加热过程所用的热交换线圈就是钽制的。 特高频无线电发射器电子管的生产用到大量的钽,钽可以捕获电子管中的氧和氮,分别形成氧化物和氮化物,从而保持所需的高真空状态。
其他用途
钽的熔点高,且能抵御氧化,所以可作真空炉部件的材料。许多抗腐蚀部件都需要用到钽,包括热电偶套管、阀体和扣件等等。由于钽的密度很高,所以锥形装药和爆炸成形弹头内层都可用钽制成。 钽可以大大提升锥形装药的装甲穿透能力。 氧化钽可用来制造高折射率相机镜片玻璃。
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

相关资料
展开
- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
知识互答
关于我们

APP下载

























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}