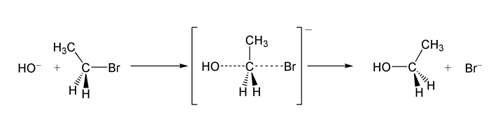
反应机理中各步的顺序也是很重要的。有些化学反应看上去是一步反应,但实际上却经由了多步,例如如下反应:
-
C O + N O 2 → C O 2 + N O {\displaystyle \ CO+NO_{2}\to CO_{2}+NO}

该反应中,实验测得的速率方程为: R = k [ N O 2 ] 2 {\displaystyle \ R=k[NO_{2}]^{2}} ![\ R=k[NO_2]^2](https://wikimedia.org/api/rest_v1/media/math/render/svg/a811d5fa67072090609159e597a93a67786e2dd6) 。因此,反应可能的反应机理为:
。因此,反应可能的反应机理为:
-
2 N O 2 → N O 3 + N O {\displaystyle \ 2NO_{2}\to NO_{3}+NO}
 (慢)
(慢)
-
N O 3 + C O → N O 2 + C O 2 {\displaystyle \ NO_{3}+CO\to NO_{2}+CO_{2}}
 (快)
(快)
每一步反应都被称作基元反应,具有特定的速率方程和反应分子数。所有基元反应加和得到的净反应必须与原反应相同。基元反应分为四类:加成、消除、取代和重排。
总反应的速率方程由反应机理中最慢的一步,也就是速率控制步骤所决定。由于上例中第一步为速控步,是一个双分子反应,速率方程为 R...


![\ R=k[NO_2]^2](https://wikimedia.org/api/rest_v1/media/math/render/svg/a811d5fa67072090609159e597a93a67786e2dd6)
 (慢)
(慢)
 (快)
(快)