



氢氧化钠
化学性质
和酸反应
氢氧化钠于水中会完全解离成钠离子与氢氧根离子,可以和酸进行酸碱中和反应:
利用这一性质,可以制备一些酸的钠盐,如:
酸性很弱的苯酚也能与之反应:
和酸性氧化物反应
氢氧化钠在空气中容易变质,就是因为和空气中的二氧化碳发生了反应:
在溶液中发生,过量的二氧化碳会将碳酸钠转化为碳酸氢钠(俗称小苏打):
由于玻璃制品中含有二氧化硅,氢氧化钠会与之反应生成硅酸钠,使得玻璃仪器中的活塞黏着于仪器上,无法再次使用。如果以玻璃容器长时间盛装热的氢氧化钠溶液,会造成玻璃容器损坏,甚至破裂的情况。
同样地,氢氧化钠也能和三氧化铬、五氧化二磷、三氧化二砷、二氧化硫、二氧化硒等其它酸性氧化物反应,生成它们的盐:
和两性氧化物及氢氧化物的反应
氢氧化钠可以和两性氧化物或氢氧化物反应,生成盐和水,如:
和单质的反应
硼、硅和两性金属(如铍、铝、锌等)和氢氧化钠反应,放出氢气:
英国在1986年有一油罐车误装载重量百分率浓度为25%的氢氧化钠水溶液,氢氧化钠便与油罐壁上的铝产生化学变化,导致油罐因内部压力过载而受损,反应方程式如下所示:
氯、溴、碘、硫、白磷等单质和氢氧化钠发生歧化反应:
和盐的反应
过渡金属的盐类和一些主族金属的盐可以和氢氧化钠反应,生成更难溶的氢氧化物,或转化为可溶性的羟基配合物再次溶解。
对于汞等氢氧化物不能稳定存在的物质来说,会生产氧化物或氧化物的水合物沉淀:
氢氧化钠可以将过渡金属的酰基离子转化为阴离子酸根(简单离子或多聚离子),如VO 2 、UO 2 等:
和其它无机物的反应
二氧化氯、二氧化氮等可以和氢氧化钠发生反应。
高锰酸钠在氢氧化钠溶液中煮沸,可以还原为锰酸钠。
和有机物的反应
氢氧化钠可以将卤代烃、酯和酰卤水解。
工业制法
氢氧化钠为工业中制氯气过程的副产物,工业上,透过电解大量饱和食盐水以量产氯气,然而,当氯离子氧化成氯气逸出的同时,溶液中也只剩下氢氧化钠一种溶质,反应方程式如下所示:
19世纪以前,氢氧化钠的制备通常会先以勒布朗制碱法生成前驱物碳酸钠,再通过高温煅烧,使得碳酸钠分解为氧化钠与二氧化碳,最后,将氧化钠溶于水中,便可制得氢氧化钠:
另外,也可利用复分解制备氢氧化钠,碳酸钠(俗称为苏打)与氢氧化钙(俗称为熟石灰)的反应方程式如下所示:
安全性

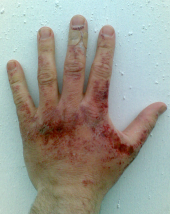
皮肤与氢氧化钠溶液直接接触所产生之灼伤,照片摄于患者与氢氧化钠溶液直接接触后44小时
氢氧化钠固体或其溶液皆能灼伤皮肤,对无防护措施者可造成永久性伤害(如疤痕)。倘若让氢氧化钠直接接触眼睛的话,严重者甚至可造成失明。个人防护措施,诸如橡胶手套、防护衣与护目镜等便能大大降低接触氢氧化钠所带来的危险。
氢氧化钠溶于水中(如稀释),抑或是与酸反应,都会放出大量的热量,可能导致灼伤或点燃易燃物(如有机溶剂)。除此之外,氢氧化钠能够腐蚀一些金属(如铝)生成易燃的氢气,还能够轻度腐蚀玻璃制品,应慎选储存氢氧化钠的容器材质。
参看
碱
氢氧根:氢氧化钾、氢氧化钙
皂化反应
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








推荐阅读
关于我们

APP下载




















