



二氧化硅
结构
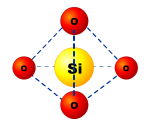
SiO 4 四面体
SiO 2 晶体有多种晶型,其基本结构单元是四面体,每个Si周围结合4个O,Si在中心,O在四个顶角;最小环上有6个硅原子和六个氧原子。许多这样的四面体又通过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。实际上, SiO 2 晶体是由Si和O按1:2的比例所组成的立体网状结构的晶体。因此,通常用 SiO 2 来表示二氧化硅的组成。 SiO 4 四面体不仅存在于 SiO 2 晶体中,而且存在于所有硅酸盐矿石中,是构成多姿多彩的硅酸盐世界的基本骨架。
物理性质
具有硬度大、耐高温、耐震、电绝缘的性能。可以透过可见光,以及红、紫外线。
化学性质
二氧化硅是酸性氧化物,对应的最高价水化物为硅酸( H 2 SiO 3 )。 二氧化硅化学性质不活泼,不容易与水和大部分酸发生反应。通常只能与碱性氧化物反应生成盐。氢氟酸( HF )是可以与之反应的酸。(还有热浓磷酸)
其与氢氟酸反应生成氟化硅的化学方程式为:
通常只能与碱性氧化物反应生成盐。例如:
与强碱反应生成盐。例如:
空气中若存在一定浓度的二氧化硅粉粒时,会经人类呼入肺部,引发呼吸器官的相关疾病,例如尘肺症。

由高纯度二氧化硅组成的光纤束。
用途
SiO 2 的网状结构决定了它具有优良的物理和化学性质,加上 SiO 2 在自然界的广泛存在,从古到今都被人类广泛地应用着。 二氧化硅与其它化合物在高温下熔融,快速冷却可以制得玻璃。它也是沙子和石英的主要成分。在半导体和太阳能板等应用中,是目前主要的原料。
仅含二氧化硅单一成分的特种玻璃叫做石英玻璃。二氧化硅与石墨或活泼金属混合可以发生氧化还原反应制得硅单质。
SiO 2 于食品工业用作抗结剂,属食品添加剂之列。
健康影响
经口摄取的二氧化硅基本上是无毒的,LD 50为5000mg / kg(5μg/ kg)。然而,吸入细分散的结晶二氧化硅粉尘可能导致矽肺病,支气管炎或癌症,因为灰尘停留在肺中并持续刺激组织,从而降低肺容量 。研究显示,暴露于结晶二氧化硅的工人比一般人群的狼疮和其他自体免疫性疾病的预期高出10倍 。在2013年发布新规范之前, 职业安全与健康管理局 ( 英语 : Occupational Safety and Health Administration ) (OSHA)允许每立方米空气100μg。 新规定将数量减少至50μg/ m 。 建筑业的暴露限值也设定为从250 µg/m 下降至50 µg/m 。
结晶形式
SiO 2 ,以比几乎任何材料都多的许多晶体形式(称为多晶型物)存在。
参阅
碳化硅
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








推荐阅读
关于我们

APP下载



















