Buchwald–Hartwig偶联反应
历史
Buchwald–Hartwig 这一类型的反应最早是由乌克兰的 Lev M. Yagupolskii 等在 1986 年发现的。他们用多取代的活化氯代芳烃与苯胺衍生物在 1mol% 的 [PdPh(PPh3)2I] 催化之下进行反应,得到了偶联产物,产率中等。
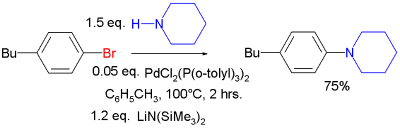
此后美国的 Buchwald 和 Hartwig 两个团队又分别在 1994 年重新发现这个反应。耶鲁大学的 Hartwig 等用的是对溴甲苯与三丁基锡基胺之间的偶联。
麻省理工学院的 Buchwald 等用的则是间溴苯甲醚与另一三丁基锡胺之间的偶联,见下。
后来又发展了第二代的 Buchwald–Hartwig 反应,即用游离胺和强碱,代替最早使用的氨基锡烷。
反应机理
反应的催化循环如下。
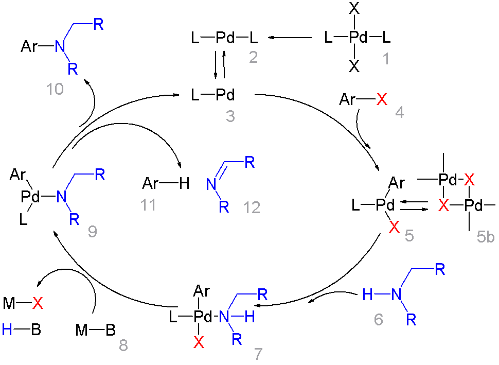
首先 Pd 催化剂 (1)被还原为活性的 Pd 物种 (2),(2) 脱去一个配体形成 (3),进入催化循环。芳卤 (4)与 (3) 发生氧化加成形成中间体 (5),(5) 与自身二聚物 (5b) 形成平衡。接下来,(5b) 中的一个卤原子被胺取代,形成中间体 (7),(7) 被强碱 (8) 去质子化,生成 (9)。然后 (9) 有两种可能的转化方式,一是发生还原消除生成需要的产物芳胺 (10),二是发生 β-氢消除生成副产物芳烃 (11)和亚胺(12)。两种情况下 Pd-L 物种都获得再生,进入下一个催化循环。
展望
对反应所用溶剂的研究发现,对于某些底物来说,甲基吡咯烷酮和二甲基乙酰胺等非质子溶剂可以促进 β-氢消除一步发生。以及非质子非极性溶剂(如间二甲苯)虽不能很好地溶解反应用碱叔丁醇盐,此类溶剂仍是此反应最好的溶剂。
参见
化学反应列表
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
知识互答
关于我们

APP下载
























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}