



肝肾综合症
分类
HRS是一种特殊的,常并发于肝硬化及爆发性肝衰竭(较少见)的肾功能衰竭。 HRS基本的病理生理学改变主要表现为肾血管收缩以及肠循环血管舒张。 基于2种不同机制的肾衰,HRS分为1型和2型,均可发生于肝硬化和爆发性肝衰竭的病例。而2种不同机制的肾衰竭均可通过血肌酐含量的上升以及肾脏内生肌酐清除率的下降来判断。腹水的生成 (如图在肝硬化病人的腹部超声上显示的黑色区域。这种腹水属于利尿剂应用无效的难治性腹水,通常产生于2型HRS
1型HRS
1型HRS主要特征是急性进展的肾功能不全,表现为血肌酐成倍增长至高于221µmol/L的水平,或者在小于两周的时间内内生肌酐清除率小于20mL/min。1型HRS的预后非常差,1月后约有超过50%的死亡率。 1型HRS的病人通常一般状况较差,可能有低血压,或者可能需要增强心肌收缩力的药物或者抗利尿激素来维持血压。
2型HRS
相反的,2型HRS相对1型来说起病和进展均较缓。2型HRS的定义是血肌酐水平超过133µmol/L,或者内生肌酐清除率小于40mL/min,以及尿纳浓度小于10µmol/L。2型HRS的前景依然不乐观,中位生存率约6个月,除非进行肝移植治疗。2型HRS被认为是一系列与门静脉高压相关的疾病谱的一部分。门脉高压最先的表现是腹腔积液,随后是利尿剂治疗无效的腹水,因为此时的肾脏已经无法排出多余的钠。许多2型HRS的病例在肾功能完全恶化之前已经出现抗利尿剂的腹水。
症状与体征
所有的HRS均由肝功能下降,循环失常以及肾衰引起。因为这三个病理生理学改变在进行到终末期之前可能不会表现出明显的症状,因此,HRS的诊断均是基于实验室检查指标的变化。多数出现HRS的患者均有肝硬化,因此可能有肝硬化相同的症状,如黄疸,肝性脑病以及营养不良和腹水。 尤其是利尿剂治疗无效的腹水是2型HRS的重要特征。肾衰时可能出现少尿,但是仍然有一些HRS病例的尿量是正常的。 因为这些症状和体征在HRS的病程中均不一定会出现,因此,他们并不是HRS的诊断标准或是诊断依据。HRS的诊断主要依据对于可能出现HRS病例的实验室检查指标,并且排出其他可能引起这些指标改变的疾病。
病因
HRS通常发生于肝硬化或者出现门脉高压的病例。虽然HRS可以发生于所有类型的肝硬化,但是研究表明其更易发生于酒精性肝硬化,尤其是经过肝脏活检证实同时伴有酒精性肝炎的病例。 HRS也可发生于急性发作的肝衰竭,如爆发性肝衰竭。
肝硬化及急性肝衰竭病人发生HRS的一些高危因素已经被确认,包括细菌感染,急性酒精性肝炎以及上消化道出血。自发性细菌性腹膜炎,一种由于腹水被细菌感染引起的疾病,是肝硬化病人发生HRS的最常见因素。在一些情况下,HRS可以在治疗肝脏疾病的并发症的过程中被引发,成为医源性的HRS高危因素,包括大剂量利尿剂的使用,通过腹腔穿刺大量抽取腹水的同时未进行足够的静脉补液。
诊断
肝硬化和爆发性肝衰竭病人发生肾衰竭有很多机制,因此,在这些肝脏疾病的病程中,判断肾衰是由于HRS引起还是其他原因引起是件非常困难的事情。因此,一些主要和次要的诊断标准被用来帮助HRS的诊断。
主要诊断标准包括:发展至门脉高压的肝脏疾病;肾衰竭;休克的出现;感染;近期肾毒性药物治疗史;体液丧失;经过1500ml生理盐水补液后肾功能仍然没有持续的改善;无蛋白尿;B超下未见泌尿系统梗阻。
次要诊断标准包括:低尿量(小于500ml/24h);尿钠低浓度;尿渗透压大于血浆渗透压,尿中无红细胞,血清钠浓度低于130mmol/L。
许多其他肾脏疾病与肝脏疾病具有相关性,因此必须在诊断HRS时予以排除。肾前性肾衰的肾脏并未收到损伤,与HRS类似,都是由于肾血流灌注不足引起。而且与HRS类似的是,肾前性肾衰时尿中钠含量很低。而与HRS不同的是,肾前性肾衰通常对补液疗法有反应,表现为血肌酐的下降以及尿钠的升高。急性肾小管坏死(ATN)是各种原因造成的肾小管的损伤,包括可能由于肝硬化治疗过程中使用的肾毒性药物以及低血压造成。由于小管的损坏,肾脏无法重吸收原尿中的钠导致尿纳比HRS高出很多,以此可鉴别HRS与ATN。 ATN还可以在尿沉渣镜检中发现透明管型以及棕色泥沙样管型,而HRS的尿沉渣镜检中则难以见到细胞管型或其他细胞组分,因为HRS时肾实质并未收到损坏。 一些病毒性肝炎,如乙型肝炎和丙型肝炎可以导致肾小球的炎症反应从而造成肾功能不全。 其他可以导致肝脏疾病患者发生肾衰的原因有:药物毒性(如庆大霉素),造影剂肾病(由于静脉内注射用于影像学诊断的增强对比的造影剂引起的肾功能衰竭)。
病例生理
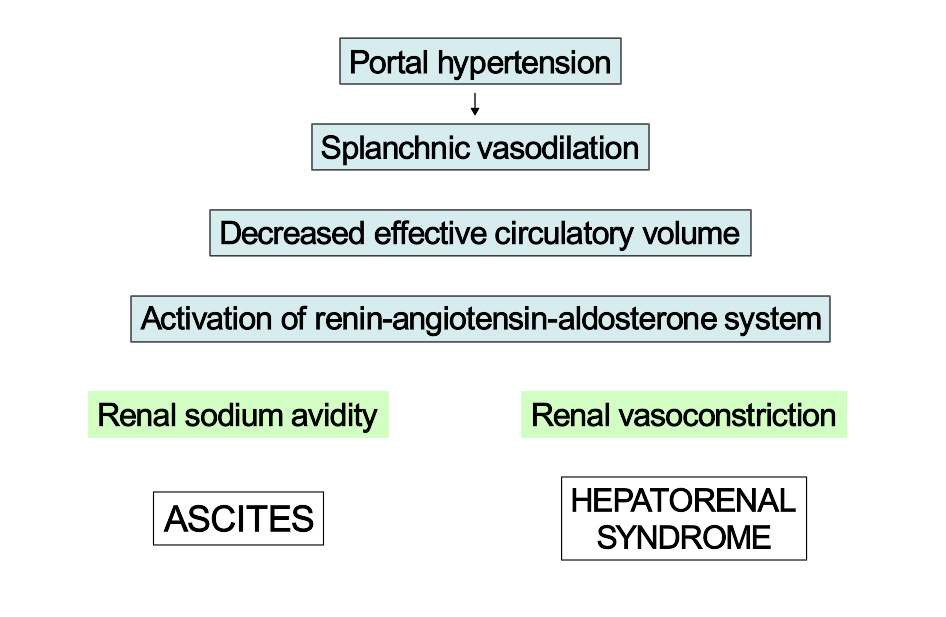
上图简要描述了产生腹水及肝肾综合征的“低灌注”理论。
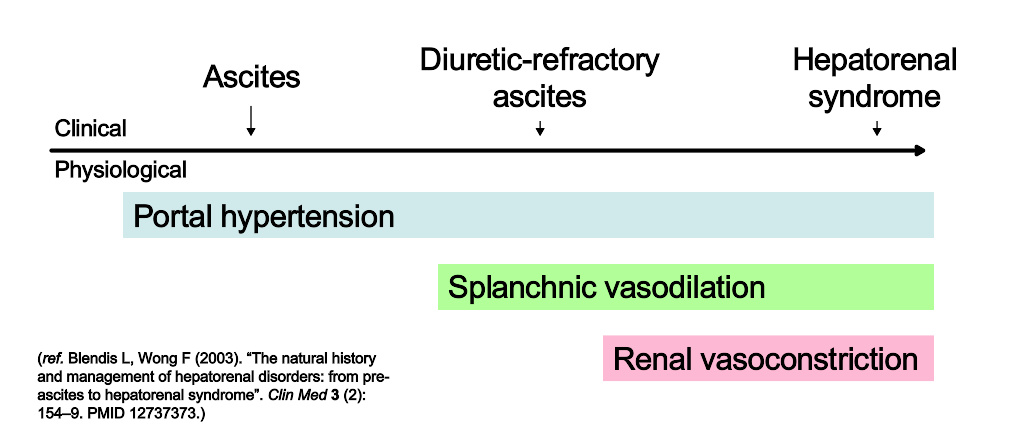
上图描述了腹水及肝肾综合征的临床表现与病理生理学变化的关联
HRS 时出现的肾衰竭被认为是肾血管紧张度发生异常所导致的。 一种普遍认同的理论认为,这种肾衰是由一些肝脏疾病所产生的因子所介导引起的内脏血管舒张(主要是肠循环血管舒张,由门脉高压所导致)和肾血管床缩窄。体内的氮氧化物(如NO)前列腺素, 等一些可导致血管舒张的因子 被高度怀疑介导了肝硬化时内脏血管的舒张。内脏血管舒张刺激肾小球近血管球体感受器,导致肾素的分泌以及肾素-血管紧张素系统被激活,全身的脉管系统收缩,尤其是肾血管的收缩更为剧烈。 然而这依然不能抵消此时内脏血管舒张所产生影响,因此,肾循环处于持续的低灌注状态,加重了肾血管的收缩,导致了肾前性的肾衰竭。
基于这个理论的定量实验显示,在HRS发生时,全身的外周循环阻力降低,然而,股动脉流量占心输出量的百分比增高,相反肾动脉流量降低,提示内脏血管舒张累及肾脏造成肾衰。许多作用与血管的因子被怀疑介导了这种全身性的血流动力学变化,包括心房钠尿肽, 前列腺环素,血栓素A2, 和内毒素. 另外研究发现,用抵抗血管舒张的药物 (如 鸟氨酸加压素, 特利加压素,善宁)治疗可以改善HRS患者的肾小球滤过率,进一步为HRS的内脏血管舒张这一发病机制提供了证据。
肾血流低灌注理论中包含了肾素-血管紧张素系统的激活,而醛固酮可以与肾脏远曲小管上的盐皮质激素受体结合,造成钠的重吸收增加, 这被认为是肝硬化腹水的发病机制中的关键过程。这个理论推测,由内脏血管舒张导致的抗利尿剂的腹水的形成以及肾血管的收缩共同导致了腹水向HRS的病程进展。
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读

关于我们

APP下载


















