碳锌电池
原电池
一个碳锌干电池是一个原电池,因为一旦电池放电完毕,不能够被再次充电而只能被丢弃。“电池翻新”曾经也出现在市场上,能够通过对电池加上一个反向电流来恢复已经部分放电的电池电量。但这些设备往往只能暂时的充电而且容易导致电池泄漏以及爆炸。与其它种类电池相比,碳锌电池之所以更容易泄漏,是因为锌同时作为放电时被消耗的负极和电池容器。锌锰电池发明于19世纪60年代,并在后来通过改进电解液形式成为干电池。
化学反应
碳锌电池的容器是一个锌罐。里面有一层由NH 4 Cl和ZnCl 2 所构成的糊状液体,这个糊状液体通过一个纸层与粉末状的碳和二氧化锰隔开。这些粉末填充在一个碳棒的周围。
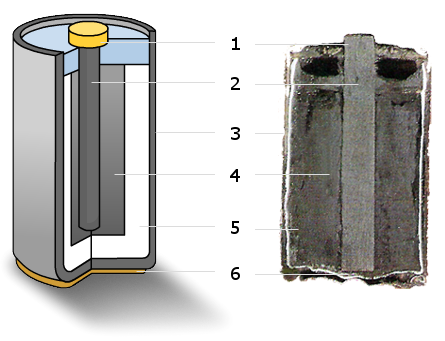
碳锌电池的横截面。1:金属帽(+),2:石墨棒(正极),3:锌外壳(负极),4:二氧化锰,5:潮湿的氯化铵糊状液体(电解质),6:金属末端(-)
在这个干电池里,最外层的锌是电池的负极。在半反应中,锌被氧化,如下式所示:
一个由粉末状碳和二氧化锰所围绕的石墨棒作为正极。其中,二氧化锰和碳粉混合是为了增加正极的导电性。阴极反应如下图所示:
H 来自于NH 4 ( aq ):
产生的NH 3 可以与Zn 结合。
在整个半反应中,锰的氧化态由+4被还原到了+3。
尽管很多副反应也可能发生,但锌碳电池的总反应还是可以由下式表示:
碳锌电池的电动势大约是1.54V。电动势的不确定是由于阴极反应十分复杂,相比来说,阳极反应(锌端)则有一个已知的电势。副反应及活性反应物的消耗直接导致电池的内阻增加,电池电动势降低。
氧化半反应:
Zn→Zn +2e
还原半反应:
2NH 4 +2e →H 2 +2NH 3
2MnO 2 +H 2 →Mn 2 O 3 +H 2 O
Zn +2NH 3 +2Cl →Zn(NH 3 ) 2 Cl 2
总反应:Zn+2MnO 2 +2NH 4 Cl→Zn(NH 3 ) 2 Cl 2 +Mn 2 O 3 +H 2 O
泄漏
当一个碳锌电池使用一段时间以后,由于金属锌被氧化成为锌离子,锌外壳会逐渐变薄。因此,氯化锌溶液常常可以从电池中泄漏出来。泄漏出来的氯化锌往往会使电池表面变粘。一些老的电池没有泄漏保护。一个锌碳电池的使用寿命比较短,保存期一般为一年半。
另外,就算电池没有使用,锌外壳也会慢慢的变薄。这是因为电池内的氯化铵有弱酸性,可以与锌反应。
氯化锌电池
高能氯化锌电池是简单锌碳电池的一个改良版,用来提供更长的使用寿命以及更稳定的电压输出。与普通锌碳电池相比,氯化锌电池的电解液不含氯化铵,由纯的氯化锌糊状液体构成。因此,阴极反应也有一些不同:
总反应如下:
环保
过去锌锰电池常加入汞以抑制负极的析氢腐蚀。出于环保考虑,中华人民共和国于2001年和2005年分两阶段对锌锰电池的含汞量作出了限制。现在,中华人民共和国出售碱性锌锰电池含汞量不高于0.0001%,碳锌电池含汞量最高不超过0.025%。不过,钮扣锌锰电池的含汞量依然没有作出要求。
参见
原电池
闪光灯电池 ( 英语 : Photoflash battery )
参考资料
Eveready:碳锌电池使用作明书
Rayovac:碱性与高能电池使用说明书
Power Stream电池化学常见问题与解答
电池组成
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








24小时热门
推荐阅读
知识互答
关于我们

APP下载
























{{item.time}} {{item.replyListShow ? '收起' : '展开'}}评论 {{curReplyId == item.id ? '取消回复' : '回复'}}