



铃木反应
概述
铃木反应对官能团的耐受性非常好,反应物可以带着-CHO、-COCH3、-COOC2H5、-OCH3、-CN、-NO2、-F等官能团进行反应而不受影响。反应有选择性,不同卤素、以及不同位置的相同卤素进行反应的活性可能有差别,三氟甲磺酸酯、重氮盐、碘鎓盐或芳基锍盐和芳基硼酸也可以进行反应,活性顺序如下:
另一个广泛应用的底物是芳基硼酸,由芳基锂或格氏试剂与烷基硼酸酯反应制备(见宫浦硼酸化反应,宫浦反应)。这些化合物对空气和水蒸气比较稳定,容易储存。铃木反应靠一个四配位的钯催化剂催化,广泛使用的催化剂为Pd(PPh3)4(0)与PdCl2(dppf),其他的配体还有:AsPh3、n-Bu3P、(MeO)3P,以及双齿配体Ph2P(CH2)2PPh2(dppe)、Ph2P(CH2)3PPh2(dppp)等。 (以上的所有Pd配体都是厌氧的,因此反应必须在氮气,氩气等惰性气体下反应)。
Suzuki反应中的碱也有很多选择,最常用的是碳酸钠,碳酸铯,醋酸钾,磷酸钾等。 碱金属碳酸盐中,活性顺序为:
而且,加入氟离子(F)会与芳基硼酸形成氟硼酸盐负离子,可以促进硼酸盐中间体与钯中心的反应。 因此,氟化四丁基铵、氟化铯、氟化钾等化合物都会使反应速率加快,甚至可以代替反应中使用的碱。
机理
反应机理见下图。首先卤代烃2与零价钯进行氧化加成,与碱作用生成强亲电性的有机钯中间体4。 同时芳基硼酸与碱作用生成酸根型配合物四价硼酸盐中间体6,具亲核性,与4作用生成8。最后8经还原消除,得到目标产物9以及催化剂1。
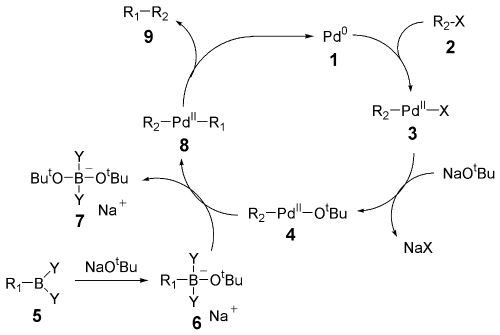
氧化加成一步,用乙烯基卤反应时生成构型保持的产物,但用烯丙基和苄基卤反应则生成构型翻转的产物。 这一步首先生成的是顺式的钯配合物,而后立即转变为反式的异构体。
还原消除得到的是构型保持的产物。
讨论
对于一些SP杂化的烷基硼或者硼酸化合物,同样可以发生反应称为硼-烷基Suzuki-Miyaura交叉耦联反应。 与铃木偶联相比它有若干缺点:1.反应进程慢;2.自身耦联副产物较多;3.和磷配体耦联的副产物多;4.可能会造成手性消旋或者羟醛缩和反应。
展望
Suzuki–Miyaura交叉耦联在有机合成当中的最新应用已经被Kotha和同事归纳。当SPhos(一种有机膦配体)参与反应,其催化剂的用量声称可以降低至0.001 mol%。
参见
Heck反应
Hiyama偶联反应
Kumada偶联反应
Negishi偶联反应
Petasis反应
Stille反应
Sonogashira偶联反应
免责声明:以上内容版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。感谢每一位辛勤著写的作者,感谢每一位的分享。

- 有价值
- 一般般
- 没价值








推荐阅读
关于我们

APP下载




















